纳米酶智能筛选新纪元 大数据驱动药物材料研发迈入临床前测试
在当今药物研发与材料科学交叉的前沿领域,一项突破性的进展正悄然改变着游戏规则。科学家们成功研发出一种创新的纳米酶筛选策略,巧妙地将大数据技术与纳米材料研发深度融合,为高效、精准的药物与材料筛选开辟了新路径。目前,该策略支撑的候选材料已顺利进入临床前测试阶段,标志着从实验室发现到实际应用的关键一步。
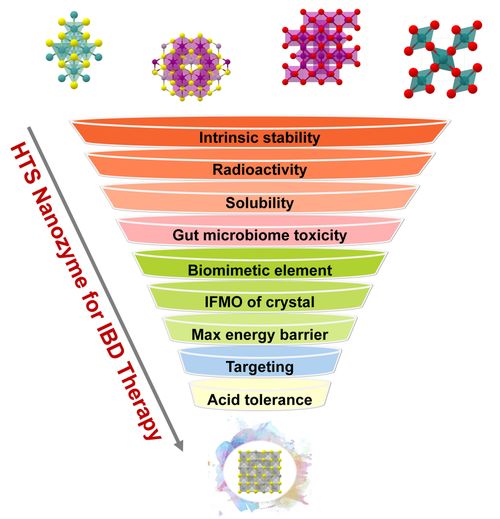
纳米酶,即具有类酶催化活性的纳米材料,因其稳定性高、成本相对较低且催化性能可调,在疾病诊断、治疗(如肿瘤催化治疗、抗菌)以及环境修复等领域展现出巨大潜力。传统筛选方法依赖于试错和有限的经验,效率低下且难以系统探索庞大的材料化学空间。如何从数以万计可能的成分、尺寸、形貌和表面修饰组合中,快速锁定高性能纳米酶,一直是制约其发展的瓶颈。
新研发的筛选策略核心在于构建一个集成化的智能平台。研究团队通过高通量实验和文献挖掘,建立了涵盖多种纳米材料(如金属、金属氧化物、碳基材料等)组成、结构参数与其催化活性(如氧化酶、过氧化物酶、超氧化物歧化酶等活性)之间关系的大型数据库。利用机器学习算法,特别是深度学习模型,对这些多维、复杂的大数据进行训练和分析。模型能够学习并推断出影响纳米酶活性的关键物理化学描述符与微观结构特征之间的隐藏规律,甚至预测尚未合成的新型纳米材料的潜在酶活性。
这一数据驱动的策略实现了从“大海捞针”到“按图索骥”的转变。科学家可以输入目标催化反应和所需的性能指标(如活性、选择性、稳定性),由模型反向推荐最有可能实现该功能的纳米材料组成与合成方案。这极大地加速了候选材料的发现与优化周期。例如,针对特定的肿瘤微环境,策略可以快速筛选出在弱酸性条件下具有高效过氧化物酶活性、能催化过氧化氢产生大量杀伤性羟基自由基的纳米酶,用于肿瘤的催化治疗。
基于该策略筛选出的明星纳米酶材料,已在实验室层面表现出卓越的性能。目前,针对某些特定适应症(如某些实体瘤或耐药菌感染)的纳米酶制剂,已经启动了系统的临床前测试。这包括严格的体外细胞毒性、药效学评估,以及动物模型体内的安全性、药代动力学和疗效研究。这些测试旨在验证其治疗潜力、生物相容性以及确定初步的给药方案,为后续可能的临床试验奠定坚实基础。
此项融合了纳米技术、酶学与人工智能的筛选策略,其意义远超单一材料的成功。它代表了一种研发范式的转变:将材料研发从经验导向转变为数据与模型驱动的精准设计。随着数据库的不断扩充和算法的持续优化,未来有望实现更广泛功能性纳米材料(不仅是纳米酶,还包括药物递送载体、成像探针等)的理性设计与高效筛选。
通向临床的道路依然需要跨越生物安全性、大规模生产稳定性、体内代谢机制明确化等多重关卡。但无疑,大数据赋能下的纳米酶智能筛选策略,已经为下一代智能药物与先进材料的研发引擎点燃了关键的火花,预示着个性化、高效能纳米医学解决方案的到来正加速成为现实。
如若转载,请注明出处:http://www.sanaikeji.com/product/60.html
更新时间:2026-01-28 13:33:36









